第一三共制药公司阿斯利康和押注新类称为抗体药物的抗癌药物配合或胜过adc——公司。今年1月,伙伴的药物Enhertu(曲妥珠单抗deruxtecan)是美国监管机构批准her2阳性胃癌,2019年药物的批准her2阳性乳腺癌。Enhertu被认为是热的东西——业内专家认为它将超过40亿美元(£28亿)一年。
对于阿兹,这些新一代抗癌药物——夫妇的瞄准能力单克隆抗体与强大的细胞毒性药物在治疗癌症——“巨大的潜力”,并承诺是大生意。一位公司发言人表示,公司致力于投资adc,目前形成的核心部分公司在癌症治疗的多管齐下的办法。我们看到一个未来adc成为治疗多种癌症的基础设置,”发言人说manbetx手机客户端3.0。
相信adc的下一件大事是癌症是一种立场许多业内人士都开始采用。自2000年第一ADC批准,这些增强抗体达到市场的10 - 7自2017年被批准。和活动空间正在蓬勃发展。去年9月看到基收购美国ADC开发者Immunomedics为210亿美元,而默克公司支付了27.5亿美元对ADC公司VelosBio 11月和12月,德国公司勃林格殷格翰集团收购了瑞士ADC公司NBE-Therapeutics€11.8亿(£10亿)。自2012年以来,已经建立了60多个合作伙伴,约有60%的交易发生自2015年以来,医药顾问根源分析报告。
与此同时,几家公司,包括英镑制药公司的解决方案,Lonza和默克公司的MilliporeSigma单元,通过收购扩大生产能力,设备采购和新建筑。这是因为ADC管道膨胀。根据根源的分析,250年左右adc目前正在开发的——在过去五年增长三倍——近40%的临床开发。可以看到这个繁荣与专利——2009年,只有1395项专利申请或批准了adc;到2019年上半年,已经达到16500多万,顾问说。早在2015年ADC市场价值约9亿美元。现在根源分析预测市场每年将增长20%以上,到2030年价值超过150亿美元。
根据顾问公司,115多家制药公司已经搬家到另一个区域的ADC的发展。新进入者进入这空间和许多公司都把巨大的努力和资本扩展他们的能力和提高他们的服务,包括战略联盟、“市场上的咨询公司在最近的一份报告中说。
这对adc的结果越来越关注癌症免疫治疗和科学进步,说安普梅农经济学人智库的高级研究分析师。过去几年的行业已经成熟批准的候选人从辉瑞,罗氏,最近,阿斯利康。这使得药物类和进一步发展的信心。考虑到巨大的潜力,越来越多的公司正在寻找交易和合作机会,他补充道。
时间轴
抗体药物配合
跳转到
1913 - 1999
从概念到现实
跳转到
2000 - 2018
adc进入市场
跳转到
今天2019 -
adc成为大企业
简史抗体药物配合
©Ella丸工作室/科学照片库
1913年
保罗•埃尔利希是神奇的子弹的概念
adc的起源可以追溯到一个多世纪,当德国诺贝尔奖得主保罗•埃尔利希提出物质结合细胞毒性载荷和约束的一个实体,专门病变细胞或有机体
1958年
第一个重大进展
ADC由甲氨蝶呤与抗体针对白血病细胞
1975年
单克隆抗体定制
塞萨尔Milstein和乔治·科勒发达的杂种细胞技术——方法生成大量的单克隆抗体的特异性。这个突破,与后抗体工程的进步,治疗性抗体的发展中心。Milstein和科勒赢得了1984年的诺贝尔医学奖
1983年
人类临床试验首次成功ADC
审判涉及ADC, thethered anti-carcinoembryonic抗原抗体对化疗药物长春地辛
1980年代——2000年代早期
安全性和有效性的挑战早期adc
许多这些问题都归因于结合战略,创建异构和不稳定的配合
2000年5月
FDA批准第一ADC
麦(罗ozogamicin)最初是由延展期间和惠氏。它是第一个治疗急性髓系白血病的新方法来市场近15年
2010年5月
麦撤回
麦罗塔ozogamicin是撤出美国市场后,新主人辉瑞临床试验提出了安全问题
2011年11月
FDA批准Adcetris
西雅图遗传学Adcetris (brentuximab vedotin)批准在美国经典霍奇金淋巴瘤复发,复发系统性间变性大细胞淋巴瘤
2017年9月
麦继续
FDA继续麦(罗ozogamicin)复发/难治性急性髓系白血病(aml)
2018年10月
FDA批准Lumoxiti
Lumoxiti (moxetumomab pasudotox)带来的总数ADC批准5。阿兹药物是第一个新的毛细胞白血病患者治疗选择超过20年
2019年
FDA批准三个adc在一年
罗氏的波利维(polatuzumab vedotin),阿斯特拉Padcev (enfortumab vedotin)和第一三共制药Enhertu(曲妥珠单抗deruxtecan)
2020年4月
FDA批准Trodelvy
Trodelvy (sacituzumab govitecan)目标Trop-2受体和用于治疗三阴乳腺癌患者,已经扩散到身体的其他部位
2020年6月
在类固醇抗
AbbVie宣布积极第二阶段试验结果abbv - 3373抗(adalimumab),抗体目标肿瘤坏死因子与糖皮质激素受体调制器类固醇——在中度到重度类风湿关节炎患者
2020年7月
阿兹和第一三共签署60亿美元的协议
阿兹同意开发ds - 1062 a人性化anti-TROP2单克隆抗体连接到一个拓扑异构酶抑制剂tetrapeptide-based链接器有效载荷
2020年9月
基同意以210亿美元收购Immunomedics
Immunomedics”投资组合包括Trodelvy (sacituzumab govitecan)
2020年9月
默克公司同意支付17亿美元西雅图遗传学
合作将开发和商业化西雅图遗传学”ladiratuzumab vedotin,试验性ADC针对LIV-1,目前在第二阶段临床试验&开发乳腺癌和其他实体肿瘤
2020年11月
默克公司获得VelosBio为27.5亿美元
VelosBio ADC发展目标受体酪氨酸kinase-like孤儿受体1 (ROR1),这是调节在各种癌症
2020年12月
勃林格殷格翰集团购买NBE疗法为€11.8亿
收购了勃林格进入NBE-Therapeutics的酶结合平台和药物候选nbe - 002, ADC ROR1也目标蛋白质
2021年1月
Enhertu批准第二指示
FDA批准Enhertu(曲妥珠单抗deruxtecan)对某些患者胃或胃食管腺癌
特洛伊木马
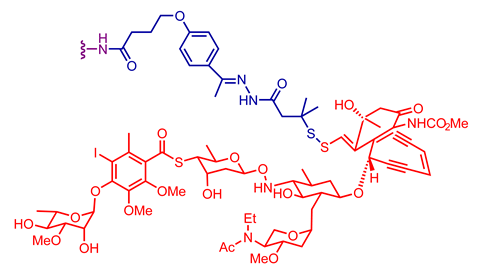
adc的承诺和潜在的双重靶向杀死作用。单克隆抗体的化合物是由共轭通过化学链接器的细胞毒性药物,称为载荷。抗体ADC指导治疗的一部分,绑定到一个特定的目标表示癌症细胞,如蛋白质HER2或CD30。复杂的性的细胞,它是退化——通过溶酶体蛋白水解作用的抗体和链接器在non-cleavable连接器或环境差异如pH值和特定的溶酶体酶可分裂的连接器。这释放细胞毒性药物,杀死细胞通过细胞分裂中断绑定或损害DNA,微管蛋白。从本质上讲,这种药物是一个特洛伊木马。这高度有效的方法允许专门的靶向治疗在肿瘤细胞的同时,仍能保留健康的细胞,不像传统的全身化疗,”阿兹发言人解释道。
但adc一直的概念,科学的复杂性导致几个失败在前几代。这是因为“早期adc遇到障碍,如高毒性和有限的功效,“阿兹的发言人说。但近期科学进步使该地区更诱人的制药公司。“最近我们看到非凡的进步与新一代adc,”该发言人说。令人印象深刻的生物工程整个行业,结合有效载荷的组合,更好的链接器技术和更好的确定目标在肿瘤生长的一个关键,是将ADC转换空间。”
简单的算术那么公司已经在拥挤的抗体癌症空间或想要打开肿瘤学的钱,梅农解释道。这些新药可能获得更好的针对病变细胞虽然保留健康的细胞,”这意味着更好的药物,巨大的潜力越好,大制药公司的吸引力。
的改进是相当重要的,解释道珍妮Craigen转化主要研究员,英国癌症研究。有一种改进的理解如何选择基于属性,如抗原的单克隆抗体亲和力和内在化是利率,而不是从现有药物开发抗体,她说。
在有效载荷的情况下,也有改进。这些细胞毒性药物,如auristatins maytansinoids,可达到1000倍比传统抗癌药物的毒性,需要非活动状态,直至肿瘤细胞释放。早期的ADC使用更强的弹头但下一代利用更广泛的有效载荷,许多显著降低效价比上一代,这可能由于ADC稳定和更好的理解方面的设计,“Craigen说。
这些新的药物可能获得更好的定位病变细胞,同时保留健康的
把Immunomedics基Trodelvy (sacituzumab govitecan),去年批准,其中包含拓扑异构酶抑制剂伊立替康代谢物SN-38, Craigen说。SN-38是一个有效载荷最大的半抑制浓度(IC50)摩尔范围低于第二代有效载荷,但高drug-to-antibody比率可以达到足够的药物在肿瘤细胞浓度。
这是链接器化学也有改善。在过去,不稳定的链接器导致过早释放载荷和不相干的毒性。而不是耦合反应使用亲核的主要氨基surface-exposed赖氨酸或减少结构的硫醇基二硫共轭链接到抗体,Craigen说更新的adc使用工程等特定站点接合侧链半胱氨酸残基或引入非天然的氨基酸。通过控制结合网站,这样可以确保adc的均匀混合物,改善drug-to-antibody比和稳定,和最小化中断抗体功能,Craigen解释道。简而言之,他们更有效的药物。
在阿斯利康的Enhertu ADC的利用新的科学小说载荷特性和链接器。澳门万博公司它是由人性化anti-HER2 IgG1单克隆抗体曲妥珠单抗,这是连接通过tetrapeptide-based劈得开的链接器一个拓扑异构酶抑制剂有效载荷,来自exatecan。药物携带大约八载荷,而大多数adc,通常携带两到四个核弹头。的属性中使Enhertu重大技术进步是高drug-to-antibody比率和链接器不仅稳定在血浆和血清也可分裂的内化到细胞,”阿兹的发言人说。更重要的是,我们相信是前所未有的,除了杀死肿瘤细胞,它已经内化,这种ADC可以目标邻近肿瘤细胞。
结果胃癌不言自明。Enhertu死亡的风险降低41%和化疗患者进行至少两次治疗,包括赫赛汀(曲妥珠单抗),缩小肿瘤,40.5%的患者,相比之下,11.3%在那些接受化疗药物伊立替康或紫杉醇。数据还表明,Enhertu-treated患者生活中位数为12.5个月和8.4个月化疗。“阿斯利康的策略是遵循科学,我们相信adc跨多个肿瘤类型有巨大的潜力,”该发言人说。
探索不同的抗体,链接器和负载组合用于选择临床批准抗体药物配合
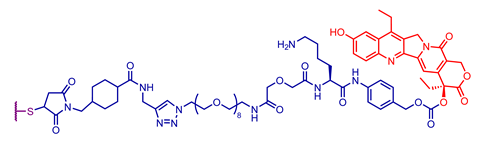
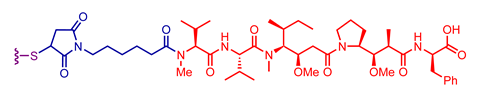
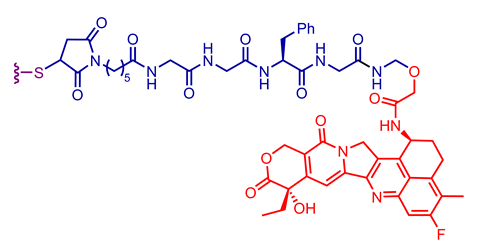
重要的外包
开发者在ADC空间也依赖外包合同制造商,因为ADC是复杂的生产,需要先进的生产能力包括细胞培养和合成化学。”并不是所有利益相关者在业界拥有端到端功能或基础设施支持的设计、开发和制造的(adc)的根源分析写道。咨询公司估计,70 - 80%的ADC制造业务外包。”这一趋势可能会在未来几年持续,”他们说,补充说,他们希望增加投资和能力在ADC生产空间进一步的科学进步。
事实上,科学是进步。当前的局限性,包括剂量优化和渗透的固体肿瘤,例如,被审查和处理。有相当大的活动到先进的结合化学反应,包括支连接器与载荷的加载多个分子的目标。与此同时,新的细胞毒性药物的研究正在进行,包括小分子RNA聚合酶抑制剂,蛋白质和酶。的几种化合物开发基于pyrrolobenzodiazepine二聚体,产生高细胞毒性DNA交叉连接,第一个pyrrolobenzodiazepine-based ADC预计在2021年被批准用于治疗弥漫型大b细胞淋巴瘤,“Craigen说。
也有积极的研究在较小的交付格式(如抗体片断和其他新颖的蛋白质结构。此外,ADC联合疗法是一个新兴的概念和研究正在结合ADC和免疫抑制剂检查站和表观遗传调节器。
最终,科学家将旨在提高ADC的治疗指数——要么通过提高ADC的效力降低最低有效剂量(如高drug-to-antibody比率)或通过改善肿瘤选择性增加最大耐受剂量。或者,在理想的情况下,在同一时间。
这些下一代药物是实质性的承诺,它超越了癌症的领域。研究已经开始adc治疗炎症性疾病,心血管疾病,新陈代谢和自身免疫性疾病。甚至还有兴趣抗菌药物,antibody-antibiotic配合使用利福霉素类似物治疗金黄色葡萄球菌已经在开发中。市场的。如果公司现在adc不感兴趣,他们很快就会。










还没有评论