迈克尔加成是有机合成中最著名的反应之一。它是一种非常有用的碳- - - - - -在不饱和羰基化合物上加入亲核试剂的碳成键反应。今天,迈克尔加物很常见,迈克尔捐赠者、接受者和加物是我们共同词汇的一部分。然而,它的发现故事同样值得众所周知,因为它标志着一个时刻,机制第一次对化学家产生了影响。

亚瑟·迈克尔于1853年出生在美国布法罗的一个富裕家庭。他的学校不教化学,但他接受私人辅导,家里还为他提供了一个实验室,在那里他进行了早期的实验。1871年,在一次前往新统一的德国的旅行中,迈克尔在柏林大学获得了奥古斯特·霍夫曼(August Hofmann)的职位,尽管他没有正式的化学资格。在接下来的9年里,他在欧洲的主要实验室学习当代有机化学,与罗伯特·本生、查尔斯·阿道夫·伍茨和德米特里·门捷列夫等人共事,也与霍夫曼本人共事。1
带着大量发表论文的记录,以及对应用物理化学原理来理解有机反应的热情,迈克尔回到了美国。在波士顿定居后,他开始了他的化学事业,其特点是充满激情的自决。尽管没有学位,他还是获得了塔夫茨学院化学教授的终身职位。在他的一生中,他在自己的实验室里进行了长期的自费研究。他经常发出批评的声音,抨击任何他认为没有根据的新理论。
在塔夫茨大学的早期,一份来自德国的报告引起了他挑剔的目光:丙二酸二乙酯钠与2,3-二溴丙酸乙酯的反应(图1)。2作者Max Conrad和Max Guthzeit提出了一种我们今天可以理解为双取代的反应:丙二酸替代了二溴丙烷酸中的两个溴,从而得到了一个含有环丙烷环的产物。环丙烷本身在19世纪80年代还是一种非常新的分子,迈克尔对此表示怀疑。
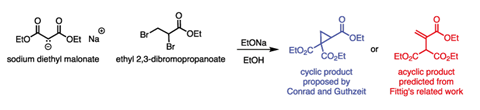
在当时,结构赋值是一件棘手的事情——唯一可用的工具是元素分析、与已知化合物进行比较以及参考文献中的先前反应。Conrad和Guthzeit的循环建议是基于William Perkin早先关于相同的丙二酸盐与1,2-二溴乙烷反应的报告。3.然而,Rudolf Fittig也报道了这种反应,并在他的案例中提出了一种无环不饱和产物。舞台已经准备好,等着有人来澄清混乱。
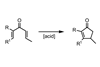
Michael认识到,与其让反应从取代步骤开始,不如让反应的第一步是失去一个溴原子作为HBr。这样就得到了不饱和分子2-溴丙烯酸乙酯。丙二酸盐会攻击-取代剩下的溴-产生非环(而不是环)产物。为了证明他的理论,迈克尔把这个过程的第二步作为他的起点——丙二酸二乙酯和2-溴丙烯酸乙酯反应。4当他得到的产物与康拉德和古策特所描述的相同时,德国人对循环产物的分配就被推翻了。果真如此吗?
迈克尔意识到他的实验有缺陷:他假设丙二酸盐会直接取代双键中溴的位置。他现在认为它可以在双键的任何一端攻击(α或β攻击),并且每条路线都可以产生不同的产物。在有人想到愤怒地画一个卷曲的箭头之前35年,他研究了这两种反应可能的中间产物和预期结果(图2),发现循环产物和不饱和产物都是可能的。
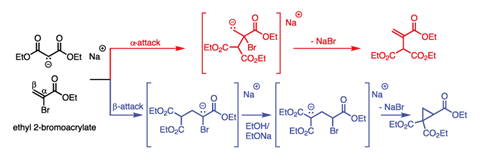
根据文献,迈克尔知道卤化氢与不饱和羰基化合物的反应有利于β攻击。因此,他提出这个反应应该以同样的方式进行,因此最终会产生循环产物。他将攻击的丙二酸盐称为“负的部分”,将双键的β-位置称为“相对正的”位置,预测了现代共轭加成电子模型。作为决定性的证据,他设计了一种已知化合物3-苯戊二酸的合成方法,只有在他的理论正确的情况下,这种方法才会起作用。这是。
于是迈克尔就这样诞生了。但并不是所有人都觉得它配得上这个名字。本文来自德国慕尼黑,5路德维希·克莱森(坚定地)指出,在他和一位名叫Telemachos Komnenos的年轻同事的工作中,有一个先例,他在四年前报告了在2-丁烯酸中添加丙二酸或丙二酸二乙酯(作为合成丁烯酸的副反应)。6迈克尔回答说,为他的论文辩护,说他的论文思想新颖;克莱森可能报道了这种反应,但迈克尔细致的调查证明了这种反应是如何起作用的。有机化学有其最早的机理研究之一。7
不久之后,迈克尔因旅行而中断了在塔夫茨的工作。作为一名艺术收藏家和古代和中世纪东方文化的终身爱好者,他在亚洲、非洲和欧洲呆了18个月。这次旅行的高潮是在英国怀特岛进行了四年的独立研究,迈克尔在那里广泛发表文章,以确定他的反应范围。8也许他这样做带有一种挑衅的意味。无论如何,他的名字保留了下来。
参考文献
1 E W福布斯,L F菲泽,A B兰姆,哈佛大学公报, 1943,38, 246年
康拉德和古特,的误码率。Dtsch。化学。全球经济。, 1884,17, 1185 (doi:10.1002 / cber.188401701314)
小W·H·珀金,的误码率。Dtsch。化学。全球经济。, 1884,17, 54 (doi:10.1002 / cber.18840170111)
4迈克尔,j . Prakt。化学。, 1887,35, 349 (doi:10.1002 / prac.18870350136)
L Claisen,j . Prakt。化学。, 1887,35, 413 (doi:10.1002 / prac.18870350144)
6 T Komnenos,贾斯特斯·李比格斯·安。化学。, 1883,218, 145 (doi:10.1002 / jlac.18832180204)
7迈克尔,j . Prakt。化学。, 1887,36, 113 (doi:10.1002 / prac.18870360111)
T Tokoroyama,欧元。j . Org。化学。, 2010,10, 2009 (doi:10.1002 / ejoc.200901130)















暂无评论