使用放射性同位素在病人体内成像——核医学——正受到老化反应堆的威胁。詹姆斯·米切尔·克罗发现了试图解决这个问题的新科学
核医学是一场与时间的赛跑。从医用放射性同位素产生的那一刻起,它就开始衰变。亚稳态同位素锝-99m (Tc-99m)是医学成像最常用的放射性同位素,其半衰期仅为6小时。尽管这狭窄的使用窗口,到10万次医学成像为了诊断从冠状动脉疾病到癌症的各种疾病,全世界每天都在使用这种短命的放射性同位素。
然而,最近,这一重要的医学分支却面临着另一个滴答作响的时钟:与时间赛跑,以支撑摇摇欲坠的医用放射性同位素供应。世界上为数不多的几座研究规模的核反应堆是Tc-99m的来源,它们中的大多数都已接近使用寿命。过去10年,老旧反应堆的意外关闭,已导致数起Tc-99m严重短缺。自2015年以来,位于法国和加拿大的两座古老的反应堆已经完全停止运行。目前,全球Tc-99m的供应量几乎全部由6个反应堆供应。
但是,在缓慢的开始之后,取代这一老化的核基础设施和保护医学成像的竞赛开始看起来我们正在获胜。新的和改进的放射性核素供应正在投产或接近完工。与此同时,医院用于成像目的的放射性同位素的范围已经多样化,通常是同步加速器而不是核反应堆制造的同位素。在生物化学方面,强大的新型放射性同位素标记分子正在彻底改变从阿尔茨海默氏症到前列腺癌等疾病的诊断和治疗。
你甚至可以说,核医学的未来似乎一片光明。
放射诊断学
如果你有一个神秘的胸痛病例,咨询医生,你可能会被送去做心脏灌注成像。这项测试用于评估心肌的血液流量,是最常见的锝-99m成像应用之一。
在瑞士苏黎世大学(University of Zurich)开发放射性药物的霍兰德(Jason Holland)说,锝是一种用于医学成像的极好的核素。他解释说:“它有140KeV的伽马射线发射,正好在你想要进行高质量成像的窗口内。”“它也是一种基于发电机的放射性核素,所以很容易获得。”

Tc-99m装在一个烤面包机大小的盒子里送到医院的影像科锝99 m生成器.它的制造过程有多个步骤,这对于20世纪50年代开创的工艺来说已经足够了,通常是从武器级铀开始的。
这种含有U-235的高度浓缩的铀被固定在一个目标上,并在核反应堆内照射。在热中子的轰击下,铀发生裂变反应,其中一种反应将铀分裂成锡-134和钼-99。Mo-99衰变为Tc-99m,半衰期为66小时,足够一个运转良好的物流系统用屏蔽的锝-99m发电机将其空运到全球各地。
在发电机内,Mo-99包含在铝填充色谱柱上。放射性同位素,以双重带电辉钼矿离子MoO的形式吸附在色谱柱上42 -,不断衰减到相应的TcO4-pertechnate离子。作为单电荷物种,TcO4- - - - - -离子与氧化铝的结合不那么紧密,可以通过标准盐水溶液通过发生器选择性地从色谱柱中洗脱。
要将放射伽马射线的Tc-99m放射性同位素转化为有用的诊断工具,需要将其与积聚在人体某一特定部位的一种分子进行协调。可能是肿瘤,也可能是心脏。
为了评估胸痛病例,医院通常使用锝螯合剂赛特米比或四福明.这些分子被心肌组织快速而选择性地吸收,在那里它们可以被Spect成像(见方框)。一旦被吸收,放射性示踪剂可以显示出由于动脉阻塞或狭窄而没有接受足够血液的心脏组织区域,指导医生确定下一个病因。
排放控制
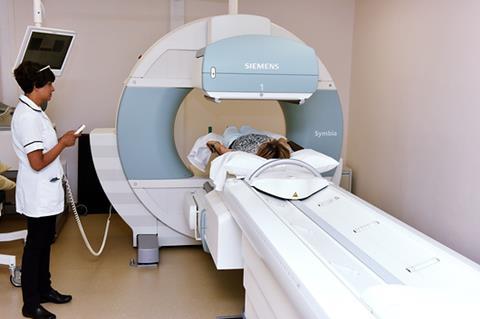
用于医学成像的放射性同位素衰变释放伽马射线——能量最高、波长最短的电磁辐射形式。高能量的伽马射线可以很容易地离开人体,并被相机探测到。发射成像的传统形式,使用放射性同位素,如Tc-99m,被称为单光子发射计算机断层扫描(Spect)。
澳大利亚墨尔本莫纳什大学(Monash University)医学成像研究员马修·迪莫克(Matthew Dimmock)解释说:“所有使用伽马射线的图像重建都依赖于必须画直线这一事实。”伽马射线沿直线传播,所以如果你能确定这条直线,你就能确定伽马射线在体内的哪个部位发出。“要画一条直线,你需要两个点,”迪莫克说。探测到伽马射线的摄像机给了你一个点。Spect成像仪器使用一个带有小孔的过滤器,称为准直器,来建立直线上的第二个点,从而能够追溯每个伽马射线的路径。迪莫克说:“当你这样做了数百万次之后,你建立的图像就变成了你在病人体内看到的图像。”
Spect成像的缺点是大部分发射的伽马射线击中准直器并被它阻挡,限制了灵敏度。而另一种发射成像技术正电子发射断层扫描(PET)却不是这样,在过去的一二十年里,正电子发射断层扫描(PET)的普及程度急剧上升。
PET同位素,包括碳-11和氟-18,通过从原子核发射正电子来衰变。一旦正电子遇到它的反粒子——一个电子,它们就会在能量爆发中湮灭,释放出一对伽马射线。迪莫克解释说:“这两种伽马射线背靠背发射,彼此180°。”身体周围的摄像头会探测到这些对,并给出绘制直线所需的空间中的两个点。没有准直器,PET成像比Spect成像灵敏度高达1000倍。
保护源
在目前生产Mo-99的6个主要反应堆中,有4个将在10年多一点的时间内达到工作寿命的终点。但其他反应堆——包括2007年在澳大利亚悉尼启用的最新的蛋白石研究反应堆——正在扩大产量。全新的反应堆预计将在未来五年内在法国、德国、韩国和阿根廷投入使用,这将有助于填补空缺。

与此同时,新的生产技术正在减少我们对核反应堆的医用同位素依赖。自加拿大永久关闭60年以来国家研究通用反应堆在2018年的乔克河,北美一直缺乏钼-99的生产,不得不进口医院所需的所有材料。尽管美国消耗了世界上大约一半的这种放射性同位素。过去10年乔克河(Chalk River)核电站意外关闭后,钼-99出现短缺,再加上人们希望在生产钼-99时不再使用武器级铀,因此美国监管机构已齐心协力培育新的钼-99生产方法。
包括美国食品和药物管理局和美国能源部阿贡国家实验室在内的组织已经与私人公司合作开拓这些新方法.2018年2月,FDA批准了第一个是由北极星医学放射性同位素研制的该公司利用来自美国研究反应堆的中子,利用中子俘获技术将Mo-98转化为Mo-99。该公司还在开发一种使用粒子加速器的无反应堆版本。使用电子加速器产生的高能光子将自然生成的Mo-100中的一个中子击出,将其转化为Mo-99。另一家公司Shine正在开发一种无反应堆的方法,该方法使用粒子加速器诱导低浓度(非武器级)铀的亚临界裂变,从而生成Mo-99。
tc - 9900万仍占全球核医学程序的80%,由于来源的多样化,其供应看起来越来越安全。另一个缓解压力的事实是,大量其他放射性同位素现在正被用于各种医学成像应用,而且还在不断增加。一些放射性同位素可以补充Tc-99m成像,其他的则可以完全取代它。
互补阵营的成像分子包含碳-11或氟-18放射性同位素。这些同位素可以用正电子发射断层扫描(PET)成像。这些放射性同位素的最大优势在于,它们可以被纳入小的有机分子中,穿过血脑屏障,从而照亮大脑中的特定结构。“这是一个不断发展的领域,”加拿大多伦多成瘾与心理健康中心成像研究中心副主任兼首席放射化学家尼尔·瓦斯德夫(Neil Vasdev)说。
阿尔茨海默症的应用
PET成像正在帮助阐明的一个主要医学兴趣领域是神经退行性疾病,如阿尔茨海默病。尽管进行了数十年的研究,但阿尔茨海默氏症缺乏任何可以减缓疾病进展的治疗方法。
直到最近,开发阿尔茨海默病药物更复杂的是,这种疾病甚至无法在活着的病人身上确诊。典型的脑损伤——萎缩的大脑结构被两种蛋白质(淀粉样蛋白和tau蛋白)团块堵塞——只能在死后才能确定。但大约15年前,美国匹兹堡大学的研究人员威廉·克伦克和切斯特·马西斯改变了这种情况。他们创造了一种基于硫黄素T的分子,用作脑组织淀粉样蛋白成像的组织学染料,并在其中加入了一个C-11原子。它被称为匹兹堡化合物B (PiB),在PET扫描中点亮淀粉样斑块。“斑块成像确实彻底改变了这一领域,”瓦斯德夫说。
我们在用碳-11和氟-18标记分子和药物方面非常有限
PiB的缺点是C-11的半衰期只有20分钟,这意味着每批最多只能用于几个病人。此后,一些淀粉样标记PET放射性示踪剂使用半衰期为2小时的F-18,已被开发出来。阿尔茨海默氏症的临床试验目前正在进行中,使用PET成像在患者出现任何症状之前识别他们,希望用淀粉样蛋白破坏药物进行早期干预,以避免这种疾病。
但像瓦斯德夫这样的放射化学家并没有固步自守。“我们研究的最大目标之一是研究淀粉样蛋白以外的PET显像剂,”瓦斯德夫说。“我们有超过10种阿尔茨海默氏症的成像方法,我们正在尝试,看看阿尔茨海默氏症的不同假设。“一种可能性是淀粉样蛋白只是疾病中的旁观者,而tau蛋白才是神经退行性变的真正罪魁祸首,因此该团队正在研究tau的PET显像剂。”
Vasdev面临的一大挑战是开发有机化学,将C-11或F-18原子合并到示踪分子中。这些放射性核素的半衰期很短,因此必须在合成的最后一步或倒数第二步加入。
“我们在用碳-11和氟-18标记分子和药物方面非常有限,”瓦斯德夫说。“对于F-18,它几乎总是与氟离子发生亲核置换。对于C-11,通常是用C-11标记的碘化甲酯或三氟化甲酯进行甲基化。我们的实验室正在努力突破我们的能力极限。”
金属离子的优点是化学反应的灵活性
Vesdev和他的团队帮助实现的一种放射性标记方法是用铜催化方法固定C-11二氧化碳,生成含有C-11标记羧酸的分子。1Vasdev和他的团队开发的另一个富有成效的领域是一种将F-18引入非激活芳香环的方法。Vasdev的改进方法从他们希望放射性氟化的非激活芳香环的相应碘化物开始。他们将碘转化为稳定的高价碘叶利德,通过与氟-18离子反应,很容易转化为所需的放射性氟化化合物。2
该团队最近使用这种策略制作了一种F-18放射性示踪剂,用于研究代谢性谷氨酸受体5 (mGluR5),该受体已知在早期阿尔茨海默病中上调。其他项目包括开发放射性示踪剂,以研究与阿片类药物成瘾和情绪障碍相关的受体。
在血液中
尽管血脑屏障对可用于大脑成像的放射性核素施加了限制,但对身体的其他部分却没有这样的限制。一些金属的同位素可以用PET成像,包括铜-64和镓-68。
霍兰德说:“金属离子的优势在于化学反应的灵活性。”“你有能力协调具有不同化学性质和不同放射性性质的不同离子,并将它们与大量不同的分子结合。”
金属被证明对肿瘤的PET成像特别有用。这个过程通常从一个分子开始,比如肽或抗体,它与肿瘤细胞表面高浓度的抗原或受体紧密结合。为了把这种分子变成显像剂,它被结合到一个螯合基团上,该螯合基团与放射性金属结合。Holland和他的团队目前正专注于开发用于前列腺癌的新型显像剂。
霍兰德说:“我们正试图找到一种新的螯合物,使我们能够以一种非常快速有效的方式协调不同的金属离子。”“我们也在寻找新的方法,将金属螯合物以特定的方式与不同的蛋白质结合。”
搜索并销毁
澳大利亚墨尔本大学的无机合成化学家保罗·唐纳利(Paul Donnelly)正试图将核医学从诊断扩展到治疗。唐纳利与罗德尼·希克斯(Rodney Hicks)建立了富有成效的合作关系,后者是墨尔本彼得·麦卡勒姆癌症中心癌症成像中心的主任。这对搭档特别感兴趣的是将诊断性放射性药物用于点亮肿瘤,并通过转换放射性核素,将其转化为高度靶向的治疗剂,直接对肿瘤进行放射治疗。
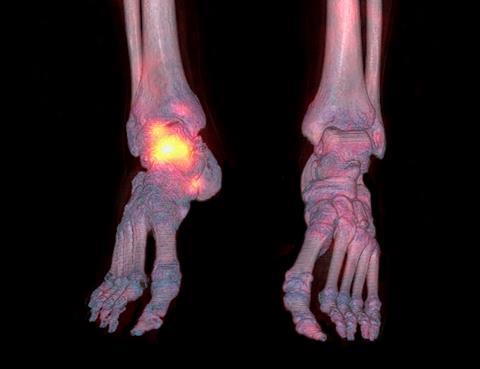
对成像有用的放射性核素发射出伽马射线,这些射线大部分穿过组织并离开身体。具有治疗肿瘤潜力的放射性核素通过释放α或β粒子衰变,这些粒子在撞击附近分子之前只移动了很短的距离。在癌症治疗中,释放的粒子通过导致DNA双链断裂来杀死肿瘤细胞。希克斯解释说:“这些粒子的路径长度为1到2毫米,所以我们可以在对周围健康组织造成最小附带损害的情况下,提供非常高的剂量。”
到目前为止,Hicks主要专注于将诊断性镓-68与治疗性镥-177配对,但他解释说,这是一种有几个缺点的组合。希克斯说:“当你标记一个生物分子时,放射性核素越大,你就越有可能改变它的生物学特征,包括对受体的亲和力。”镓-68和镥-177有相似之处,但不是同一种金属。另一个缺点是镓-68的半衰期只有68分钟。“我们只能模拟细胞吸收这种生物分子的早期阶段,我们无法确定这种分子在肿瘤中的保留程度。”
一个更好的诊断-治疗组合是使用一些铜放射性核素。铜-64已经用于PET成像,其12.7小时的半衰期足以用于图像摄取和随后的放射性药物清除。同时,铜-67是一种具有极好的治疗潜力的β粒子发射器,希克斯说。由于两种标记的放射性药物的体内行为应该是相同的,使用PET成像来跟踪前者的摄取和清除将允许非常精确地给后者加药,这一过程被称为定量前瞻性辐射剂量测定。
希克斯说,唐纳利开发的新化学物质对这项工作至关重要。3.以前的铜螯合剂不能很好地结合铜,并且会缓慢地泄漏金属。希克斯说:“以前的尝试都是注定要失败的,因为如果Cu-67脱落,它将辐射到正常组织,而不再是肿瘤。”
Donnelly采用了一种已知的铜螯合剂,一种被称为石蜡的大双环己胺笼状配体,并对其进行了修饰,特别是开发了一种可以可靠地连接到Hicks正在研究的肿瘤靶向肽上的胺的坠羧酸基团。肽结合生长抑素受体过度表达在许多类型的神经内分泌肿瘤。唐纳利说:“在我们找到罗德向他提出这个想法之前,我在化学方面研究了至少五年。”希克斯立刻意识到其中的潜力。在临床前测试成功后,该团队现在正在进行首次人体试验。
大量的费用用于处理核反应堆产生的废物
与此同时,唐纳利和他的团队正在研究其他靶向生物分子,以标记铜放射性核素。唐纳利说:“我们有一种连接剂和螯合剂,我们一直在研究如何将其连接到你想要的任何生物分子上。”项目包括一种针对与一些乳腺癌病例相关的HER2受体的抗体。Hicks补充说,靶向前列腺特异性膜抗原来治疗前列腺癌是铜治疗放射化学的另一个潜在途径。
目前,Cu-67的供应有限,研究小组必须从美国爱达荷州立大学的线性加速器中获取放射性核素。“人们说,‘你不能得到Cu-67,那为什么要为它开发一种放射治疗剂?希克斯说。“但当我开始做镥疗法时,只有一家可靠的供应商,而现在有一大堆供应商。他说,Cu-67没有理由不会发生同样的情况。“如果我们正在进行的治疗试验是积极的,我们证明了这项技术的实用性,将会有更大的动力将Cu-67生产过程工业化。”他补充说,世界各地的其他粒子加速器没有理由不能开始生产这种粒子加速器。
事实上,就诊断而言,我们没有理由不能把所有的程序都转换到粒子加速器产生的放射性核素上,而不是在核反应堆中,希克斯说。4“处理核反应堆产生的废物需要花费大量的成本,此外还有安全问题和环境问题。“相比之下,回旋加速器产生的放射性核素非常便宜,在绝大多数情况下都没有废物。希克斯说:“它们应该被使用,这是显而易见的。”对我来说,这应该是不可避免的。
詹姆斯·米切尔·克罗是澳大利亚墨尔本的科学作家
参考文献
1 B H罗斯坦等,ACS医学化学。列托人。, 2014,5, 668 (doi:10.1021 / ml500065q)
2 B H罗斯坦等,Commun Nat。, 2014,5, 4365 (doi:10.1038 / ncomms5365)
3 B M帕特森等,道尔顿反式。, 2014,43, 1386 (doi:10.1039 / c3dt52647j)
4 R J希克斯,M S Hofman,Nat. Rev. clinin。肿瘤防治杂志。, 2012,9, 712 (doi:10.1038 / nrclinonc.2012.188)










暂无评论