随着一种含有氘的药物即将获得批准,妮娜·诺特曼对氘化药物的前景进行了调查
一旦进入体内,药物分子必须在冲向生物目标的过程中躲避代谢系统的猛烈攻击。人体致力于将药物分子迅速粉碎成不活跃的小碎片,然后将它们排出体外,这意味着许多药物需要比正常情况下更频繁地服用。
有人提出了一种使天平向有利于药物的方向倾斜的方法,即用更重的氘取代分子中的一些氢原子。碳-氘键比氢键更强,导致反应速度的差异可达6到10倍。因此,如果C-H键的断裂导致药物的代谢比理想情况更快,那么用氘代替氢可能会减缓分子的分解。最终的结果是,这种药物可以减少服用次数,一天一次而不是两次。
因为氘是氢的同位素,这种原子替换不会改变分子的形状、大小、电荷或生物效应。只有药代动力学,即药物如何在体内移动,应该改变。这样做不仅可以改善药物半衰期:更少的药物-药物相互作用,减少患者之间分子代谢的变异性,还可以提高耐受性。
氘已经被广泛用作一种同位素标签,用于在实验室和人体中研究候选药物的代谢。然而,到目前为止,它还没有被用于最终的药物分子。但这种情况可能即将改变。目前看来,首个氘化药物即将获得批准。2015年8月,梯瓦制药工业公司(Teva Pharmaceutical Industries)申请在美国销售一种含有6个氘原子的药物分子。审批过程通常需要10个月左右。
放慢节奏
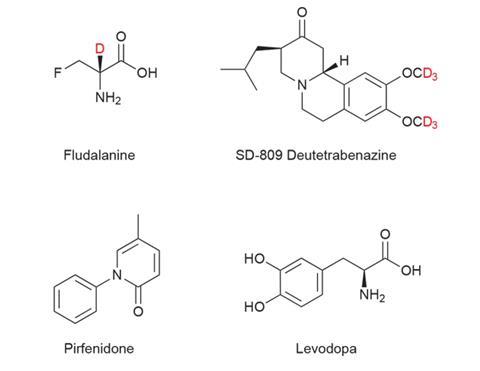
几十年来,使用氘来保护药物免受不必要的新陈代谢的想法一直在幕后酝酿,20世纪70年代,美国制药公司默克公司将第一种氘化药物投入临床试验。分子fludalanine或者3-氟-2-氘d-丙氨酸具有抗菌特性,但在IIb期试验中出现脑毒性问题,导致该项目的工作停止。毒性与氘无关。
氘化的效果有很大的差异,从非常有益到毫无益处
大约十年前,当Auspex制药公司(现为Teva所有)、Concert制药公司和Protia公司开始为已知药物的氘化类似物申请大量专利时,获得市场批准的努力再次开始升温。
“这是个好主意。你只需改变药代动力学,你就知道药物会起作用,因此你就降低了药物开发过程中的风险,”美国新墨西哥大学对同位素效应感兴趣的药学科学家Graham Timmins解释道。“唯一的风险是,你的临床效果不会大到足以说服别人花很多钱。”
问题就在这里:C-H断裂只是药物代谢的多种方式之一,而弄清楚药物的代谢途径(以及氘的放置位置)并不总是那么简单。蒂明斯说:“你会发现,氘化的效果有很大的变化,从非常有益到什么都没有。”放置不当的氘甚至会加速药物分解。
梯瓦的候选药物目前正在接受美国FDA(食品和药物管理局)的审查,是SD-809,也被称为氘化四苯那嗪或deutetrabenazine.自20世纪60年代以来,四苯那嗪一直被用作抗精神病药。今天,它被批准的用途之一是治疗与亨廷顿舞蹈病相关的舞蹈病(不自主运动)。这是梯瓦寻求批准使用其氘化类似物的第一个迹象。
双四苯肼在两种强迫症中含有六个氘原子3.芳香环上的基团。梯瓦公司报告说,在母体分子中,C-D键的强度是C-H键的8倍,这种取代显著增加了药物在体内的半衰期,并具有其他优点,包括提高安全性和耐受性。
美国制药咨询公司Recondite Falls Discovery的托马斯·甘特(Thomas Gant)说:“因为我们在第一阶段的临床试验中看到氘化化合物和蛋白质版本之间的巨大改进,人们忍不住说,‘哇,这真的有很大的不同’。”甘特是Auspex的科学创始人,但后来离开了该公司。
双四苯那嗪也在试验中用于治疗运动障碍——运动障碍和图雷特氏综合征——而未氘化的母体分子四苯那嗪在美国没有被批准用于这两种适应症,但在世界其他地方却有。这种氘化药物目前正在美国、英国和欧盟进行针对运动障碍的III期临床试验。梯瓦表示,他们希望在2016年申请美国食品药品监督管理局(FDA)对这种情况的批准,但美国以外的计划细节尚未公布。
梯瓦在2015年5月收购Auspex时表示,到目前为止,该公司已经确定了大约60种潜在的氘化候选药物。氘化的pirfenidone(sd - 560)左旋多巴(SD-1077)是另一个最先进的分子。
总部位于以色列的Teva公司斥资35亿美元(25亿英镑)收购了Auspex公司,这清楚地表明该公司相信,利用氘来增强已知药物的纯度是有利可图的。梯瓦表示,他们预计至少在2031年之前,他们将在美国拥有获得的分子的独家经营权。关键的是,所有的利润都是他们一个人的:目前,这些分子未氘化类似物的任何仍然有效的专利的所有者都看不到。
提高合规
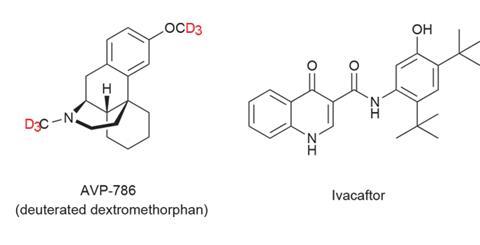
总部位于美国列克星敦的Concert的氘化药物项目也吸引了大量投资和兴趣。该公司最先进的药物是AVP-786,是与Avanir Pharmaceuticals(最近被日本制药商大冢制药公司收购)合作开发的。AVP-786是止咳药的氘化类似物右美沙芬,两个甲基都完全氘化。
自2011年以来,右美沙芬在美国也被批准与奎尼丁治疗假球效应,一种通常被描述为情绪失禁的情况,可能由于神经系统疾病或脑损伤而发生。在这种组合中,奎尼丁的作用是减缓右美沙芬的代谢。但是奎尼丁的副作用对于有心血管危险因素的患者来说是值得关注的。
Avanir现在发现使用AVP-786可以减少奎尼丁的用量,因为氘也可以减缓右美沙芬的代谢。较少的奎尼丁意味着较少的心血管副作用。AVP-786/奎尼丁组合药物正在进行治疗阿尔茨海默病患者躁动的III期临床试验,并在美国进行治疗重度抑郁症和精神分裂症的II期临床试验。
这是氘修饰改变化合物药代动力学的一个展示
协和公司也在开发氘改性ivacaftor(Vertex Pharmaceuticals以Kalydeco的名称销售)。Ivacaftor是一种新药,2012年首次在美国获批,2013年在英国获批,用于治疗囊性纤维化。这就是Concert正在测试其氘化类似物的迹象。
第二阶段试验计划在今年晚些时候开始。Concert首席执行官Roger Tung解释说:“我们正在完成该建筑群的第一阶段项目。”“这很好地展示了氘修饰改变现有化合物药代动力学特性的能力。”
Ivacaftor每天服用两次,与高脂肪食物一起服用,有助于吸收。“对Kalydeco的坚持似乎不是完全理想的,”Tung说。“我们希望通过简化给药方案,能够提高囊性纤维化患者对药物的粘附程度,并从中获得临床益处。”“目前还没有关于Vertex公司如何看待这个药物研发项目的消息,因为如果成功了,可以合理地假设它将对ivacaftor的利润产生连锁反应。”
手性控制
与此同时,位于美国安多弗的DeuteRx公司正在从不同的角度开发氘化药物。他们没有改变药物的药代动力学,而是使用氘来控制分子的手性。DeuteRx首席执行官希拉·德威特(Shelia DeWitt)解释说:“我们正在使用氘手性开关外消旋药物,这种药物是作为混合物开发的,因为两种对映异构体可以相互转化。”“通过在手性中心放置氘,我们发现能够减缓外消旋化,从而获得所需对映体的立体选择性或立体富集。”
他们的标志性方法是在羰基旁边的手性中心放置一个氘,以阻止烯醇中间体的形成。“通常情况下,在基本环境中,手性中心α到羰基的质子会被抽象出来。平面的中间产物烯醇可以被两侧的水淬灭,从而引起消旋。”她解释道。由于C-D键比C-H键更强,氢/氘取代减慢了烯醇的形成。
有很多先例表明单一对映体总是比混合物好
德威特和她的团队已经证明了这种技术可以为投资者赚钱。她的第一家氘化药物公司Deuteria Pharmaceuticals在2012年以4200万美元的价格将一种化合物的知识产权卖给了Celgene。这是Celgene公司抗癌药物来那度胺的氘化版本,是一种外消旋混合物年代而且R通过烯醇中间体相互转化的对映体。自购买以来,氘化类似物的开发进展的细节尚未宣布。
德威特说:“有很多先例表明,单一对映体总是比混合物更好。”“无论何时服用一种由两种化合物混合而成的药物,并选择其中一种对映体,在药代动力学方面总是有好处的。”
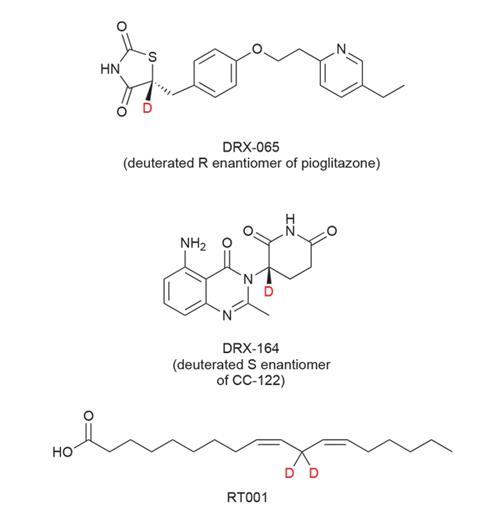
DeuteRx的先导化合物DRX-065是氘化的R抗糖尿病药物的对映体吡格列酮这是一种外消旋药物,在一系列其他适应症中也显示出有益的作用,包括罕见的遗传性神经退行性疾病肾上腺白质营养不良(ALD)。这就是DeuteRx为DRX065所追求的条件。它的临床前研究表明年代吡格列酮的对映体是导致药物增重副作用的原因。”R对映体表现出所需的线粒体功能调节和抗炎活性,没有[副作用]。德威特说:“我们计划在今年第三季度将DRX-065用于人体临床试验。”
DeuteRx公司不仅希望改进已获许可的药物,他们还在对其他制药公司仍在研发中的候选药物进行氘化。DRX-164是氘化的年代德威特解释说:“Celgene在临床试验中有一种候选药物的对映体,称为CC-122。”CC-122是另一种沙利度胺类似物,有望成为来那度胺更有效、更安全的版本。DRX-164仍处于临床前研究阶段。
专利的担忧
这也就不难理解为什么这些初创企业和资助原始药物开发的大型制药公司之间存在不和。一旦这些药物开始进入市场并赚大钱,事情可能会变得更加激烈。
“假设一家大型制药公司获得了一种非仿制药的非氘化版本的专利。然后另一个人获得了同一种药物氘化版本的专利。如果专利已经过期,那么大型制药公司就没有理由试图起诉。蒂明斯说,但如果他们获得了有效的专利,那么看看结果如何将会很有趣。“氘化后的药物不会100%氘化。它可能只有99%的氘化,那么该公司将出售1%的东西,这是由另一个人的专利覆盖的。同样,品牌公司的药品,也会有一些自然生成的氘。他们出售的产品会受到对方分子的一丝污染。”
大型制药公司正在为氘化版本申请专利,这样其他人以后就不能申请了
为了避免这种情况,许多大型制药公司开始为他们管道中所有药物的任何可能有趣的氘化类似物申请专利。蒂明斯说:“大型制药公司宣称这些产品是氘化的,这样其他人以后就不能宣称它们是氘化的。”
辉瑞就是这样一家希望以这种方式保护其资产的公司。辉瑞的药物代谢化学家Alfin Vaz解释说,在辉瑞的大多数药物开发项目中,都考虑到了氘化的潜力。他说,我们的大部分努力都是为了看看氘能否改变药物清除时间。
保护辉瑞的知识产权可能是这项工作的主要目的,但不排除未来开发氘化药物的可能性。“我们所发现的所有(氘化)对化合物有帮助的研究都没有进展是因为其他原因,而不是因为药代动力学。”也许有一天,我们会出于某种原因提出氘化版的药物,但目前还没有这种药物。”
除了大型制药公司从一开始就能更好地保护自己的资产外,蒂明斯预计,小公司最终会发现,要在美国获得现有药物氘化类似物的专利将变得更加困难,因为专利局将开始声称这种想法缺乏新创性。
但Concert的Tung说,这还没有发生:“我们现在能够继续获得专利,总体上比我们最初遇到的困难少了很多。很常见的情况是,最初的反应是基于新鲜感而拒绝。然后,我们会告诉审查员,为什么我们声称的这组化合物与其他化合物具有不同的性质,而这些可能是基于现有技术所无法预测的。”
不同的方法
Retrotope是一家美国氘化药物公司,没有人会指责它缺乏新意,也没有人会指责它不踩别人的脚。这家位于洛斯阿尔图斯的初创公司正在使用氘来稳定一种膜脂肪酸,以对抗一种自然致病的化学反应:氧化。脂质过氧化,脂质的氧化降解,被认为是包括阿尔茨海默病和帕金森病在内的许多疾病的可能原因。
亚油酸它是一种多不饱和ω -6脂肪酸,是细胞膜的主要成分。这是一种必需脂肪酸,必须从食物中获取,因为人体无法合成它。亚油酸有两个双键由一个CH分开2组。“这个点通常是一个弱点,因为那些双键想要被共轭,但它们没有。Retrotope的首席执行官罗伯特·莫利纳里解释说:“当氢原子在那个位置被(活性氧)剥离时,它就变成了自由基——它被共轭了。”然后,这种自由基与另一种脂肪酸反应,然后与更多的脂肪酸反应,直到最终被熄灭。
他说:“我们专注于阻止这一事件,因为它既启动了整个级联反应,又导致它传播到致密膜中其他易受影响的分子。”Retrotope的主要药物是RT001,亚油酸,在两个双键之间的碳上有两个氘原子。这种分子是口服的,通过天然脂肪酸过程到达细胞膜。
2015年8月,针对弗里德里希共济失调(一种罕见的遗传性疾病,会对神经系统造成进行性损害)的首次临床试验开始了。Molinari说:“我们现在已经完成了第一批低剂量的试验,目前高剂量的试验已经进行了一半。”
在弗里德里希共济失调中,铁结合蛋白frataxin的表达减少导致线粒体内表面的游离铁。游离铁是亚油酸过氧化反应的催化剂。“在线粒体内部产生活性氧的地方有游离铁,就像在焊接车间里有未经加工的气体。这让疾病发展得更快,”莫利纳里说。“虽然我们不能改变线粒体中铁的含量,但我们能做的是让启动这整个潜在的自动催化过程的脂肪抵御激进的攻击。”
几十年的氘化药物审批之路似乎即将结束,梯瓦的SD-809似乎最有可能获得第一个批准。从最初希望延长药物清除时间开始,制药公司现在发现氘在药物分子中的广泛潜在用途。在未来,我们在当地药店的货架上看到的越来越多的药物中都可以看到氘的身影。
尼娜Notman是一位生活在英国索尔兹伯里的科学作家







1读者的评论