将小分子药物与聚合物结合可以为药物研究人员提供巨大的回报
这个理论是合理的:你把一种传统的小分子药物,然后把它附着在聚合物上,你就会得到一种新的药物(聚合物-药物缀合物),它会有更长的寿命在活的有机体内血浆半衰期比单独用药要短(图1)。
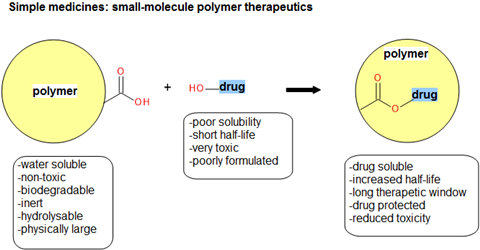
聚合物药物是制药行业的沃土,因为它们不需要研究新的活性药物成分(api)或新的聚合物。公司内部的常绿制药部门甚至可能有机会进一步开发知识产权。而且,对于临床医生来说,使用一种API众所周知的药物是有信心的,这种药物多年来已被用于多种疗法中成功治疗许多患者群体。
小分子制剂的进步使得制药公司寻求获得长释放(改性释放或缓释)制剂的知识产权在一种新药被鉴定出来之后。仅作为止痛药,FDA就批准了35种品牌或仿制的“缓释或长效阿片类药物”。1对于小分子聚合物治疗来说,情况则完全不同。自20世纪60年代末基于聚合物的药物出现以来,在任何医学领域,都没有得到批准的小分子聚合物疗法。
快速浏览一下FDA的“橙皮书”或英国国家处方集(两者都是药物参考来源),就会发现新型小分子药物的长效配方是常规的东西。但小分子聚合物疗法的长效等价物却无处可寻。小分子聚合物药物是否可行?
更好,更便宜…
聚合物偶联产品具有明显的医疗优势,如降低毒性,增加半衰期,更好的药代动力学/生物利用度和增强的药物溶解性。新实体是足够新颖和不明显的知识产权,因此它既可以作为一个离散的结构,也可以作为专利权利要求书中马库什结构描述的集体的一部分。在这些疗法中使用的聚合物受到严格的定义,以获得高质量的产品。它们必须无毒、水溶性、生物惰性,对药物具有某种形式的物理保护,并通过水解链接与小分子结合。此外,当与小分子药物连接时,它们不能附着在潜在的作用位点上,并且必须是完全可生物降解的(图1)。
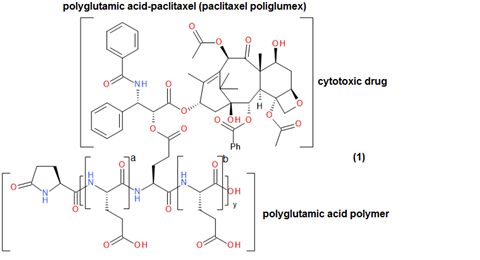
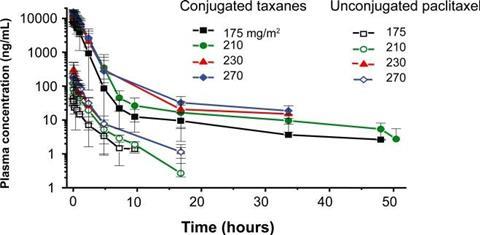
这方面的一个例子是聚谷氨酸(PGLA)-紫杉醇(紫杉醇poliglumex),这是一种小分子聚合物研究药物,在治疗一些癌症疾病方面表现出了希望(图2)。2在患者中,与单独使用紫杉醇相比,它表现出溶解度增加、药物逐渐释放、半衰期延长、静脉给药更迅速和更大的被动肿瘤积累。与未结合的紫杉醇相比,这种小分子聚合物缀合物能够在较长时间内(在多种药物剂量强度下)表现出更高的血浆浓度(图3)。然而,紫杉醇poliglumex仍未获得FDA批准作为任何医学适应症的药物。2
聚合物共轭产物在技术上也更便宜。成本是最初药物发现研究的主要决定因素,而小分子药物的发现非常昂贵,在美国估计每年为1.3亿美元。3.由已知聚合物和现有小分子原料药组成的药物的成本基本上为零,从而规避了最初的发现成本。然而,尽管有这些潜在的节省,还没有批发制药兴趣开发小分子聚合物治疗。
但仍然不受欢迎
有大量的文章和报告促进聚合物药物作为一个不断增长和进步的治疗类。4目前有近40种小分子聚合物疗法正在进行临床或临床前评估,其中19%处于II期和III期,26%处于I期或II期。到2026年,预计将有8种新药物获得批准,其中两种将是重磅药物,来自目前正在评估的小分子药物偶联物。这无疑将为这类疗法令人兴奋的未来奠定基础。4
对这一“好消息”进行更严格的分析表明,聚合物药物的主要贡献来自生物分子的递送,如酶、蛋白质、脂质体和单克隆抗体。事实上,在目前批准的聚乙二醇(PEG)治疗药物中,有14种是PEG与大分子生物分子耦合的药物,而只有一种是小分子(纳洛西戈l),其中PEG不是传递聚合物,而是作用机制的固有部分。8个候选人中有多少人获得批准,有多少人将在第一阶段、第二阶段或第三阶段消失,目前还有待猜测。进一步的分析表明,只有少数制药公司参与了小分子聚合物治疗研究。然而,最令人痛苦的现实来自药物银行统计数据,该数据显示,2337种小分子药物被批准用于医疗用途,但没有一种被批准为聚乙二醇化小分子药物。5
开处方的临床医生在这里确实扮演着重要的角色,因为他们会通过修改释放和缓释配方,常规地开出成熟的小分子药物的长效变体,以增加患者的治疗窗口,尤其是在药物的半衰期很短的情况下。这正是那种支持小分子聚合物疗法作为日常长效疗法的环境。然而,一旦患者开始对小分子药物反应良好,就没有什么动力将他们转移到更新的小分子聚合物治疗方法,除非现有的药物出现了问题——正如俗话所说,“如果它没有坏,就不要修复它”。
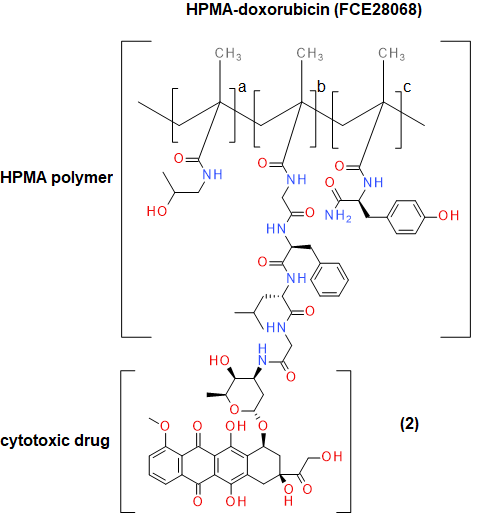
小分子聚合物疗法总是排在小分子疗法之后,除非有迫切的需要使用它们。有这种临床需求的一个例子是在临床试验中N-(2-羟丙基)甲基丙烯酰胺与阿霉素偶联(图4)得到相应的共轭。它已被用于治疗乳腺癌、肺癌和结直肠癌。6治疗性蒽环类衍生物(如阿霉素)的主要副作用是快速发生心脏毒性作用,以充血性心力衰竭(CHF)的形式,导致50%的死亡率。7目前接受阿霉素抗癌治疗的患者不能治疗CHF的效果。研究表明,hpma连接的阿霉素大剂量(1680mg/m)的心脏毒性降低了五倍3.)显示在低浓度(80-320 mg/m)时没有心脏毒性和抗肿瘤活性3.).6
HPMA聚合物-阿霉素缀合物的使用在临床研究中引起了极大的兴趣,因为在临床医学中没有更安全的阿霉素使用治疗方案。然而,再一次,这种小分子聚合物缀合物仍然没有找到成为批准药物的调控途径。
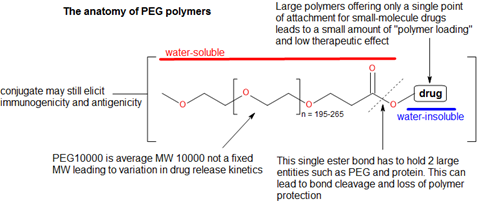
然后是整个聚合物偶联结构本身的问题,这似乎是一个不稳定的结构,两个大的成分,如蛋白质和聚合物,由一个单点水解键连接在一起(图5)。毫不奇怪,这种键容易过早断裂,释放药物和聚合物,而没有任何半衰期延长。在聚乙二醇聚合物中发现的另一个问题是,药物只能在一个单点上缀合。这提供了非常差的负载能力,这限制了如果只能将一个分子添加到PEG链上所能达到的功效。虽然聚合物被认为是生物惰性的,但在动物和人类研究中都发现了抗原性和免疫原性反应。8、9从化学的角度来看,将不溶于水的有机药物与溶于水的生物聚合物结合是相当困难的。在化学中,处理这类分子缀合的合成程序很少,它们对在研究环境中实现小分子聚合物治疗提出了严重的障碍。其他化学问题与聚乙二醇聚合物的平均分子量有关,而不是固定分子量。这导致长链和小链与小分子药物缀合,但具有不同的药物释放动力学。10这一领域的偶然观察者可能会注意到,似乎只有少数聚合物被认为是“生物聚合物”。PEG, PGLA和HPMA似乎在这一区域占主导地位,但其他的呢?
最后,“聚合物”仍然是指“工业聚合物”而不是“医用聚合物”。一般来说,聚合物似乎是其自身成功的受害者,因为在医疗领域,它们可能被视为生物聚合物材料,而不是生物聚合物药物。在相关的发展中,聚合物疗法现在不得不应对一个新的竞争者。碳纳米管(CNT)的研究领域已经从学术上的好奇迅速发展成为现代药物输送的首选答案。这使得许多人从聚合物药物缀合物转向制造功能化纳米管。11
可行的治疗?
对于蛋白质、抗体、酶和脂质体等生物分子,答案显然是肯定的。许多利用聚合物增强药物传递的生物分子已被批准。然而,小分子的情况有所不同。目前还没有系统的方法来制造已批准的小分子药物的聚合物版本,就像改性或缓释制剂一样,小分子聚合物疗法的发展缓慢(或不存在)。除非没有其他选择,否则临床医生可能不会使用小分子聚合物疗法。制药公司大多选择远离,不认为聚合物是药物发现或常青的机会——尽管聚合物疗法的开发可能更快、更便宜。
无论如何,我们不能放弃小分子聚合物疗法。新的候选药物目前正被积极评价,并被吹捧为大片,因此不能被忽视。帮助药物研究人员熟悉小分子药物偶联物领域可以打开这整个领域。关于小分子聚合物药物的专门信息源可以提供一个涵盖化学、药物信息和知识产权等困难领域的多功能数据库。这还不存在,但可以作为这一领域所有研究人员的焦点。它还可能改变人们对小分子聚合物疗法的态度,使它们被视为小分子的长效改性和缓释变体,并以相同的速度发展。
小分子聚合物疗法背后的强大理论基础为您的组织提供了一个探索的好机会,特别是在这个领域目前竞争有限的情况下。
下载PatSnap的指南解密马库什结构或观看PatSnap与《化学世界》合作举办的网络研讨会,manbetx手机客户端3.0”在专利中找到化学黄金的简单方法
参考文献
1.www.fda.gov /药品/ DrugSafety / InformationbyDrugClass / ucm251735.htm
2.SD Chipman等人,Int。j .纳米, 2006: pmcid:2676644
3.https://www.liaison.com/blog/2017/05/02/cost-drug-development/
4.https://www.prnewswire.com/news releases/dendrimers -和-聚合物药物配合-市场- 2016 - 2026 - 300294316. - html
5.https://www.drugbank.ca/stats
6.LW Seymour等人,Int。j .杂志。, 2009, doi:10.3892 / ijo_00000293
7.K Chatterjee等人,心脏病学, 2010, doi:10.1159 / 000265166
8.J Tsuji等人,Int。j . Immunopharmacol。, 1985, doi:10.1016 / 0192 - 0561 (85) 90158 - 4
9.RP Garay和JP Labaune,打开会议进程J。, 2011, doi:10.2174 / 2210289201102010104
10.www.thermofisher.com(2018)。什么是聚乙二醇(PEG)?[网上]可于以下网址索取:https://www.thermofisher.com/us/en/home/life-science/protein-biology/protein-biology-learning-center/protein-biology-resource-library/pierce-protein-methods/polyethylene-glycol-peg-pegylation-proteins.html
11.AMA Elhissi等人,j .药物。Deliv。, 2012, doi:10.1155 / 2012/837327








暂无评论