BRSM说,去对称性提供了一种巧妙的方式来添加棘手的特征澳门万博公司
尽管在过去的一个世纪里,有机合成化学取得了很大的进步,但仍有一些结构特征会让经验丰富的化学家望而却步。澳门万博公司本科生的教条认为,小环(少于5个原子)、中环(7到8个原子)和全碳四元立体中心是坏消息。但是,虽然在规划路线时确实需要一点额外的考虑,但它们已经不像50年前那样是噩梦了。
也就是说,很少有好的通用方法来制作它们,这是一种遗憾。特别是第四纪中心,在自然产物中大量存在,现在重要的不仅是能够形成它们,而且是立体选择性地形成它们。事实上,如果它们能更容易地构建成分子,我们可能会看到它们在以平坦著称的药物化学世界中更频繁地出现——考虑到含有它们的生物活性天然产物的数量——这可能是一件好事。
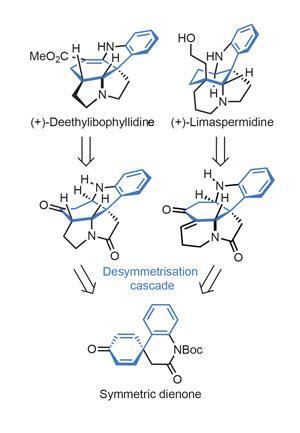
应对这些挑战的一种越来越不常见的方法是去对称性。想法很简单——制造一个对称的分子,这通常很容易,然后打破这种对称。主要的缺点是,这通常只设置一个立体中心,而且它通常不是特别有用的产品。然而,这两个问题都已被克服Chun-An风扇他在中国兰州大学(兰州大学)的研究小组进行了两项研究的综合夹竹桃科使用去对称级联反应的生物碱(图1)。
天然产品爱好者无疑会认出这个家族,因为它给了合成界一些最喜欢的目标——以及几种临床使用的药物。的确,利血平,aspidophytine和长春花生物碱都来自这一组植物。
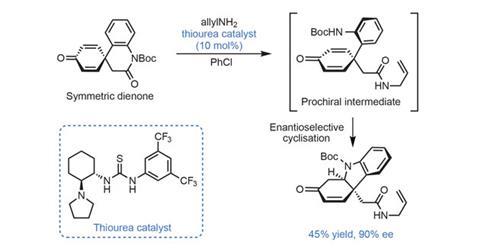
有点不同寻常的是,团队的关键步骤实际上是在路线的最开始,有足够的时间和材料来优化它。级联反应包括首先用伯胺打开内酰胺。在双功能硫脲催化剂的引导下,从这个氨解步骤中弹出的受保护的苯胺,可以选择性地在两个前手性二烯烯烃中的一个上进行环化(图2)。收率只有45%,但有一句古老的谚语说,产率一般的最佳位置是第一步(或最后一步),该小组巧妙地利用这个反应中的氢咔唑产物来制造这两种目标天然产物。
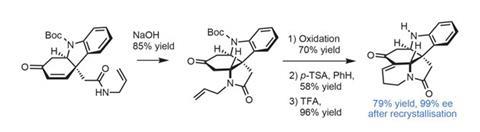
接下来,用氢氧化钠处理使酰胺在烯酮上发生环化,形成倒数第二个环。在钯催化下,烯丙基氧化为醛,酸介导的醛醇与附近的酮缩合完成了五环核心。在这一点上,该团队最终获得了一种中间体,可以重新结晶,将对映体过剩一直提高到99%,而没有明显的材料损失(图3)。
从这一点来看,只有少数官能团操作完成(+)-利亚脒,尽管在酰胺的化学选择性还原方面遇到了一些麻烦,需要一些意想不到的步骤。
对于(+)-去乙基libophyllidine,该组从去对称反应中得到产物并将其转化为类似的酮。不需要的羰基随后被燃烧掉;下面的酮Barton-type Wolff-Kishner条件,与酰胺配合氢化铝锂.然后在Swern条件下对仲胺进行化学选择性氧化,得到的亚胺用Mander试剂酰化(甲基cyanoformate)和二异丙酰胺锂(乔治。)来提供目标天然产物。
祝贺这个小组的新方法——我很有兴趣看看这是否适用于这个重要家族的其他成员。
BRSM (@BRSM_blog)是一名博士后研究员博主总部设在美国








暂无评论