通过吡咯的痛苦工作
当你在寻找一个目标或在合成中提取中间产物时,某些官能团会让你心一沉。它们可能会与过渡金属结合,当你不希望它们反应时,它们会反应,使提纯复杂化——或者有时以上都是。有趣的是,药物化学家有一个专门的术语来描述这些危险的功能:pain(来自泛化验干扰化合物)。这个词起源于一项开创性的研究2010年的论文上面列出了已知会混淆高通量屏幕的官能团,这样研究人员就可以避免这些麻烦了。1
我不知道合成化学家也有类似的名单,但经验(我和同事的经验)让我对不止几个化合物类保持警惕。我有四唑,它们与钯紧密结合以至于可以将它们形成的配合物列出来。非六价硫对氧化非常敏感,而且相当烷基化——直到你需要裂解二硫烷保护基团的那一刻。即使是像羧酸和胺这样的基本物质,也很难通过最短的合成序列,除非它们有保护基团。
一个更隐蔽的家族是富电子的五元杂环,尤其是吡咯。Oxidisable吗?非常!亲核的?检查!合理的酸性质子?是的,它对酸也很敏感,因其特有的火红色分解产物而得名。理论上,纯吡咯是无色的,但我从未见过不是深棕色或黑色的瓶子,因为它总能找到反应的物质。吡咯既是痛苦又是痛苦。
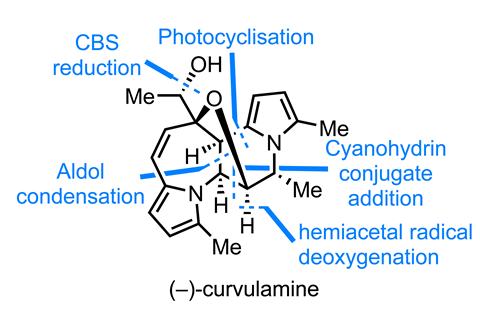
我会小心翼翼地处理哪怕只含有一种吡咯的天然产品,所以我对它印象特别深刻最近的合成双吡咯曲柳胺的汤姆Maimone以及美国加州大学伯克利分校的同事。2该基团的合成始于共轭添加一个氰醇酰基阴离子,相当于一个不同寻常的10π吡咯氮平酮。n -碘琥珀酰亚胺捕获产生的烯酸盐。乍一看,这个阴离子的加入似乎是为了两个烯酮中反应性较弱的那个,但记住,吡咯的电子密度并不在氮上——它在邻近的碳上质子化。
接下来,一个有趣的光循环,让我想起了经典的维特科普吲哚耦合。最初,该小组试图通过单电子还原剂和光氧化还原催化来还原烷基碘化物以实现自由基环化。这些反应产生了少量的产物,但远不如不使用催化剂,用正确波长的LED灯照射底物时产生的产物多。这种事情发生的频率比你想象的要高,所以一定要记得运行那些控制反应!
加入锂化乙基乙烯醚(第二个酰基阴离子等价物),就能得到目标中的最后两个碳原子,研究小组只需再做一点立体化学和氧化态杂凑,就能取得胜利。首先,甲氧基钠可以使吡咯和乳酸之间的甲基立体中心异构化。它最初是作为一种外聚物的混合物生成的,但是大多数不需要的外聚物与碱的平衡会优先生成所需的结构,次要的外聚物可以在以后的合成中循环使用。
然后,该团队可以燃烧掉不需要的乳酸羟基,只需要减少剩余的酮就可以完成目标。然而,当暴露于常见的氢化物还原剂时,底物对生成与所需构型相反的酒精的坚定偏好几乎阻碍了这一过程。使用完全等效的手性Corey-Bakshi-Shibata催化剂克服了这种选择性,并方便地将外消旋酮分解为一对可分离的、近对映纯的非对映体之一的(-)-曲戊胺。
最近,我看到迈蒙就这项工作发表了一篇悲叹的演讲,它远没有论文看起来那么简单。所以恭喜这个团队,他们最终充分利用了吡咯的固有反应性,同时避开了它产生的众多陷阱。
参考文献
1 J B贝尔,G A Holloway, J.医学化学。, 2010,53, 2719 (doi:10.1021 / jm901137j)
2 K T Haelsig, J Xuan和T J Maimone,j。化学。Soc。, 2020,142, 1206 (doi:10.1021 / jacs.9b12546)










暂无评论