印度科学家的一项新的理论研究声称提供了压倒性的证据,证明最简单的碳化合物,双原子碳(C2),有一个四键。研究人员认为他们的发现可以通过实验来验证。对于这样一个有争议的领域,该领域的一些专家仍然不服气,这并不奇怪。
“有些问题永远不会消失。“碳二聚体中化学键的性质,特别是由于碳有四个价电子,使用它们与另一个碳原子形成四键的可能性最近引起了很多讨论,”量子化学家评论道耶稣Ugalde他来自西班牙巴斯克地区大学,并没有参与这项研究。
分子轨道和价键理论的方法通常提供了相互矛盾的结果,关于碳的键序2,前者通常预测双键,后者通常预测四键。现在,Debashree Ghosh,Ankan保罗和印度科学培养协会的研究生Ishita Bhattacharjee采用了一种新的基于分子轨道理论的方法来解开化学键。高希说,他们在研究中使用的方法并不新鲜,但“我们使用的方式是我们认为非常新颖的”。
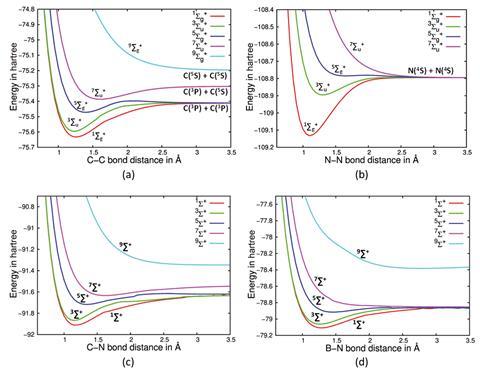
高希、保罗和巴塔查尔吉分析了C的低自旋西格玛态的势能曲线2,以及其他二聚体如N2, CN+和乙炔。在C的七重态中找到一个深度最小值2他们说,这是潜在四重键存在的证据,并为实验验证打开了一扇窗口。“所有其他方法都会给你一个特定的数字,这个数字本身不是特征值,这就是为什么它不是一个可观察到的。如果它不是可观察到的,它就永远不会在实验中被捕捉到,”保罗解释说。高希说:“这里唯一的问题是,你实际上必须将这个分子激发到高自旋状态,而且它必须有点稳定,至少在实验上可以探测到它。”
“C2众所周知,这种分子是非常不稳定的,但我们确实在另一个物种CN中发现了四键特征+保罗说。他解释说,自从科学家最近分离出CN+在离子阱中,它增加了研究其激发电子谱的机会。“我们希望能有一些实验来揭示C语言结合的这一方面。2”。
自旋unpairing
该团队提出,他们可以通过确定产生纯解离势能曲线的自旋对称性值来确定第二行二聚体在基态下的键数。他们依赖于一个古老的概念,化学键是两个原子核共享的分子轨道上的自旋电子对,这可以追溯到刘易斯一个多世纪前做出的开创性贡献。然后,通过逐渐自旋解成对电子对,他们认为他们一次消除一个键。这是通过计算更高的自旋态得到的。导致纯解离势能曲线的那个应该对应于“无键”,因此实现这种纯解离势能曲线的步骤数可以与键的数量相关联,”Ugalde说。
这出现在C的非净自旋对称中2(与N2和乙炔),他们认为这是因为C的两个原子之间有更多的键2.研究小组相信他们的结果为C2,有两个σ键和两个π键。
物理化学家马可Nascimento来自巴西里约热内卢de Janeiro联邦大学的,对这种方法有保留意见:“如果为了定义一个分子的基态,必须检查同一分子的激发态,那么化学结构的概念有多大用处呢?”
保罗说:“我们确实理解人们从激发态势能曲线的角度来解释基态成键场景时可能会有的担忧。”“如果我们考虑烯烃中的E-Z异构化,这个想法可能就不那么陌生了,这在光化学方法下很容易实现。”当我们注意到基态中两个碳原子之间的双键不能在基态中轻易异构化,而不能在激发态中围绕单键自由旋转而轻易异构化时,我们对基态中两个碳原子之间的双键有了更好的理解。从本质上讲,我们的方法建立在对多重绑定的简单理解之上,以理解C中的复杂场景2.与单键分子相比,多键物种的光谱学更丰富,这也不是巧合,因为激发态本质上是基态键的结构。”
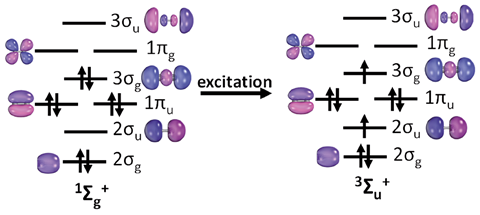
乌加尔德说,这是对计算债券订单难题的一个值得称赞的贡献。“然而,这与检查最低自旋态的轨道并确定它们是否对应于成键、反键或非成键相互作用不同。波函数,因此轨道,针对特定的自旋状态进行了优化,因此不同于任何其他自旋状态……我们还没有说出最后一句话关于这个问题的确切答案。”
“自旋态的改变会在一定程度上改变轨道,”保罗回答说。“尽管存在这个问题,当工作中建议的标准应用于一系列第二周期二聚体时,它符合传统的键序,同时适用于C2它预测了四重键。然而,我们承认这个想法的强度必须在几个系统上进行测试,以及其他现有的系统,以检查它的稳健性。”



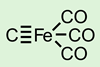

暂无评论