瑞典和意大利的研究人员推导出了一个方程,说明了范德华半径和电负性如何作为压力的函数相互关系。1“这种联系已经被暗示了很长时间;这在某种程度上是非常直观的。如果电子离原子核更近,它们就更容易被束缚,原子就更小,电负性也更强。马丁·拉姆瑞典查尔姆斯理工大学教授,他领导了这项研究。
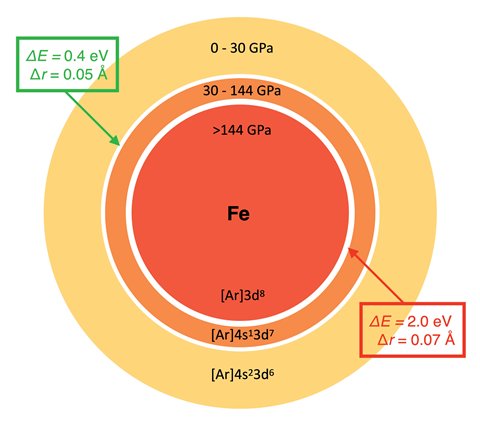
在之前的研究中,2、3Rahm和他的同事们使用密度泛函理论结合极压极化连续模型,计算了93个原子在0到300GPa压力下的范德华半径和电负性。他们最近将这些数据,以及自旋和基态电子构型汇编到一个应用程序中。已知压力可以诱导许多原子的基态电子构型的跃迁,以及它们Atoms-under-pressure应用强调了在这种跃迁中原子半径和电负性预测的尖锐不连续。通过探索非键合原子在给定压力下在竞争电子态之间转换的标准,Rahm的团队现在推导出了一个有关原子半径和电负性的方程。他们说,例如,这个表达式可以帮助解释在环境条件下降低原子的氧化态如何降低其电负性,以及反之亦然在氧化。
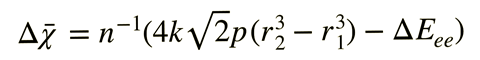
其他科学家已经报道了将电负性与压力下的原子半径联系起来的框架,但Rahm说,这些框架通常只适用于少数原子——不系统地横跨周期表,而且通常不提供给定的压力。他解释说:“我们花了很多精力来建立一个与可测量的东西相对应的模型,我们给出了在给定压力下的这些特性。”Rahm设想,研究人员可以将他团队的数据集用于高压结构预测(例如获得单位细胞体积的良好初始近似)、定义压缩系统中的分子数、识别键合原子和性质预测等领域。不过他也承认,在压缩条件下使用原子性质可能会更加困难:“成键与基本原理的混乱程度将决定它们的用处。”
“这是一个重要的贡献,”计算化学家说Pratim Kumar Chattaraj来自印度理工学院卡拉格布尔。然而,Chattaraj警告说,“结构、成键和反应性在密闭条件下会发生剧烈变化。”所有原子或分子性质的变化可能不会遵循相同的趋势,因此在自由状态下有效的相关关系在受限情况下可能不成立。”
参考文献
1 M·拉姆,P·埃哈特,R·卡米,化学。科学。, 2021, doi:10.1039 / d0sc06675c(本文是开放获取的。)
拉姆先生等,ChemPhysChem, 2020,21, 2441 (doi:10.1002 / cphc.202000624)
拉姆先生等,j。化学。Soc。, 2019,141, 10253 (doi:10.1021 / jacs.9b02634)








暂无评论